Leis da Reações Químicas
Introdução
As Leis das Reações Químicas, deduzidas de forma empírica por cientistas como Lavoisier, Proust e Dalton, nos permitem calcular quantidades de substâncias presentes nas reações, bem como estabelecer relações matemáticas entre as quantidades. Estas leis foram formuladas antes mesmo de se conhecer teorias sobre ligações químicas e estrutura eletrônica e serviram de base para a
Teoria Atômica Clássica. São elas:
• Leis ponderais - aquelas que se referem às massas das substâncias;
• Leis volumétricas - aquelas que se referem aos volumes dos gases.
Leis Ponderais
Lei de Lavoisier: Lei da conservação da massa
Publicada pelo químico francês Antoine Laurent de Lavoisier,em 1789, no “Tratado Elementar de Química” e também chamada de Lei da Conservação da Massa ou Lei da Conservação da Matéria. Esta lei afi rma que:“Na natureza nada se cria, nada se perde, tudo se transforma.”
“A massa total de um sistema fechado não varia, qualquer que seja a reação química que aí venha a ocorrer.”
“Numa reação química, a soma das massas dos reagentes é igual à soma das massas dos produtos.”
• Exemplo:
Observe a conservação da massa na reação química entre o sulfato de alumínio e o hidróxido de cálcio:
Al2(SO4)3 + 3 Ca(OH)2 → 3 CaSO4 + 2Al(OH)3
342 g + 222 g = 408 g + 156 g
A soma das massas de reagentes é igual à soma das massas de produtos, ou seja, 564 g.
Lei de Proust: Lei das proporções constante
Formulada em 1801, pelo químico francês Joseph Louis Proust, é também chamada de Lei das Proporções Defi nidas, Fixas ou Constantes. A lei de Proust estabelece que:
“Em uma determinada reação química, realizada em diversas experiências, a proporção entre as massas dos reagentes ou produtos é constante.”
“Uma determinada substância pura composta, independente de sua procedência, apresenta sempre a mesma composição em massa dos elementos constituintes.”
A Lei de Proust permite a determinação da composição centesimal de uma substância e o cálculo estequiométrico.
• Exemplo:
Observe a proporção constante entre as massas de ferro e enxofre que se combinam em três experimentos para produzir sempre sulfeto ferroso:

O valores numéricos em cada proporção foram divididos pelo menor deles, resultando sempre na proporção de 1,75:1,00.
Lei de Dalton: Lei das proporções Múltiplas
Também conhecida como lei de Dalton, diz que quando dois elementos reagem formando substâncias diferentes, se a massa de um dos dois permanecer constante, a massa do outro irá variar segundo valores múltiplos ou submúltiplos.
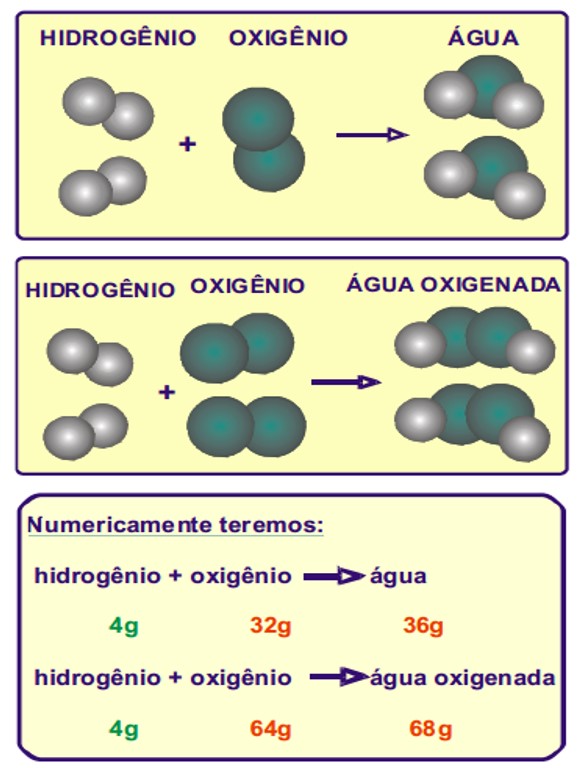
A massa do hidrogênio foi mantida constante e as massas do oxigênio são valores múltiplos.
Lei volumétrica de Gay-Lussac
Formuladas em 1808, pelo físico e químico francês Joseph Louis Gay-Lussac, serviram para a consolidação da Teoria Atômica Clássica, afirmam que:
“Quando medidos nas mesmas condições de temperatura e pressão os volumes dos reagentes gasosos em uma reação química formam entre si uma proporção de números inteiros e pequenos.”
• Exemplo:
Observe a relação entre os volumes gasosos medidos nas mesmas condições de temperatura e pressão para os participantes da reação a seguir:

Os valores numéricos em cada proporção foram divididos pelo menor deles, resultando sempre na proporção de 1:3:2.
Note que essa proporção coincide com os coeficientes da equação química balanceada.
